Dérivez le tableau périodique de façon expérimentale
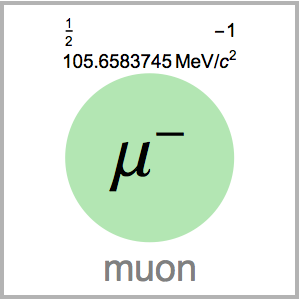
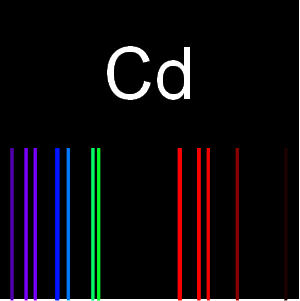
La relation entre la périodicité des propriétés élémentaires et la structure électronique atomique sous-jacente peut être difficile à visualiser. Pour étudier la relation entre le nombre quantique principal et l'énergie d'ionisation, vous pouvez examiner la première énergie d'ionisation correspondant aux 54 premiers éléments. Si la supposition est correcte, les premières énergies d'ionisation devraient tomber dans des groupes basés sur le nombre quantique principal, 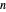 , de l'électron le plus éloigné.
, de l'électron le plus éloigné.
La propriété "IonizationEnergies" renvoie une liste, il suffit donc d'extraire la première énergie d'ionisation.
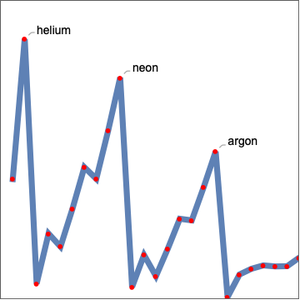
Comme prévu, les premières énergies d'ionisation se répartissent en cinq groupes correspondant au nombre quantique principal. L'énergie d'ionisation n'est pas la seule propriété élémentaire présentant une périodicité. Examinez le rayon atomique pour les mêmes éléments.
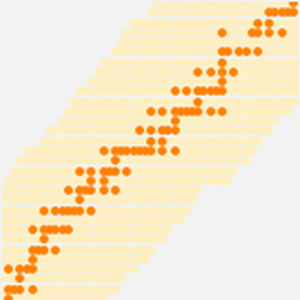
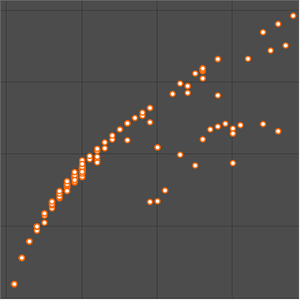
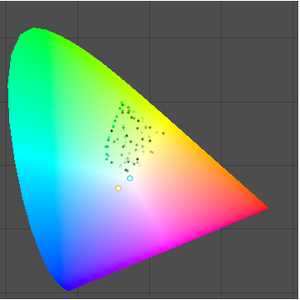
Les données sur le rayon atomique se répartissent en groupes encore plus nets, en corrélation avec le numéro quantique principal de l'électron qui se trouve le plus éloigné de l'atome. Les regroupements des nombres quantiques principaux observés suggèrent une structure organisationnelle fondée uniquement sur les données expérimentales observées. Pour mieux visualiser cette organisation potentielle, faites pivoter les données du rayon atomique, désactivez les légendes des données et ajustez le rapport d'aspect du graphique obtenu.
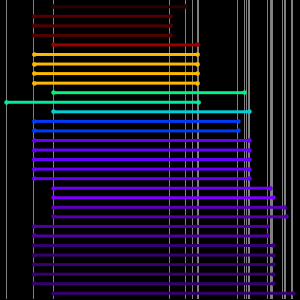
On obtient cinq "rangs" inclinés contenant respectivement 2, 8, 8, 8, 18 et 18 éléments. En aplatissant les rangs et en espaçant un peu, on peut voir que la forme standard du tableau périodique moderne commence à apparaître.